Rote - Hand - Briefe
Rote - Hand - Briefe
 CredibleMeds®
CredibleMeds®
 Springer Medizin - Das Fachportal für Ärzte
Springer Medizin - Das Fachportal für Ärzte


Arznei aktuell
ifap Service-Institut für Ärzte und Apotheker GmbH
Bunsenstraße 7 · 82152 Martinsried München
Telefon (0 89) 244 09-119
Telefax (0 89) 897 44-300
eMail info@ifap.de
Internet www.ifap.de

21. Mai 2026
Informationsbrief: Chargenrückruf Yimmugo
Rückruf der Charge C795945P03 (3er-Bündelung) & C795945P04 Yimmugo, 100 mg/ml Infusionslösung 100 ml, Verfallsdatum 31.05.2028.
 mehr...
mehr...

13. Mai 2026
Neue Therapieoption bei Status epilepticus
Mit Fosphenytoin ist jetzt ein neues Arzneimittel zur Kontrolle des Status epilepticus verfügbar.
 mehr...
mehr...

12. Mai 2026
Rote-Hand-Brief: Cenobamat
Risiko für schweren Leberschaden und neue Empfehlungen zur Überwachung der Leberfunktion bei Anwendung von Ontozry.
 mehr...
mehr...

11. Mai 2026
Rote-Hand-Brief: Tecovirimat-Monohydrat
Tecovirimat SIGA: Einschränkung der Indikation aufgrund mangelnder Wirksamkeit bei Patienten mit Mpox.
 mehr...
mehr...

8. Mai 2026
Rote-Hand-Brief: Progesteron
Fehlerhafte Kennzeichnung der äußeren Umhüllung in der Blindenschrift bei FAMENITA 200 mg Weichkapseln, 90 St. (N3).
 mehr...
mehr...

4. Mai 2026
Rote-Hand-Brief: Fosphenytoin
Risiko von Medikationsfehlern und Off-Label-Anwendung bei Kindern unter 5 Jahren bei Fosphenytoin Desitin 75 mg/ml.
 mehr...
mehr...

28. April 2026
Rote-Hand-Brief: Bendamustin
Risiko von Medikationsfehlern bei Bendamustin Accord Konzentrat zur Herstellung einer Infusionslösung 25 mg/ml.
 mehr...
mehr...

14. April 2026
Lieferengpässe bei Holoxan, Endoxan, Phenhydan
Lieferengpässe bis 2026/2027: Onkologische Therapien und neurologische Notfallbehandlung müssen frühzeitig angepasst werden.
 mehr...
mehr...

10. April 2026
Rote-Hand-Brief: Naltrexon/Bupropion
Mysimba®: Information zu langfristigem kardiovaskulärem Risiko und neue Empfehlungen für die jährliche Bewertung.
 mehr...
mehr...

1. April 2026
Lynkuet® zur Behandlung vasomotorischer Symptome
Mit Lynkuet® steht der erste duale Neurokinin-1-/Neurokinin-3-Rezeptorantagonist in der EU zur Verfügung.
 mehr...
mehr...

31. März 2026
Rote-Hand-Brief: Gebrauchsinformationen
Risiko für Patientensicherheit durch nicht zulassungskonforme Gebrauchsinformationen (Dr. Friedrich Eberth Arzneimittel).
 mehr...
mehr...

27. März 2026
Rote-Hand-Brief: Iohexol und Iodixanol
Risiko von Partikeln in Accupaque Injektionslösung (Iohexol) und Visipaque Injektionslösung (Iodixanol).
 mehr...
mehr...

20. März 2026
Informationsbrief: Chargenrückruf Yimmugo
Rückruf der Chargen C795395P01 & C795395P02 (3er-Bündelung) Yimmugo, 100mg/ml Infusionslösung 100ml, Verfallsdatum 31.01.2028.
 mehr...
mehr...

19. März 2026
Rote-Hand-Brief: Phenytoin-Natrium
Phenhydan® Injektionslösung (Phenytoin-Natrium): Risiko von Partikeln Aktualisierung der Information vom 07.11.2025.
 mehr...
mehr...

12. März 2026
Neuer SERD zur Brustkrebstherapie
Inluriyo® bietet Erwachsenen, die an bestimmten von Formen von Brustkrebs erkrankt sind, eine neue Behandlungsoption.
 mehr...
mehr...

27. Februar 2026
Methenamin-Hippurat: neu bei wiederkehrenden HWI
Mit Cystohipp® steht erstmals ein Präparat mit Methenamin-Hippurat bei wiederkehrenden Harnwegsinfekten (HWI) bereit.
 mehr...
mehr...

13. Februar 2026
Verzögerung des Typ-1-Diabetes
Mit Teizeild® ist die erste krankheitsmodifizierende Therapie bei Typ-1-Diabetes auf dem Markt verfügbar.
 mehr...
mehr...

6. Februar 2026
Rote-Hand-Brief: Fondaparinux Natrium
Schwerwiegender Qualitätsmangel bei Arixtra im Zusammenhang mit der Nadel in der vorgefüllten Spritze.
 mehr...
mehr...

2. Februar 2026
Informationsbrief: Ribociclib
Änderung der Lagerungsbedingungen und Haltbarkeit für das Produkt Kisqali® 200 mg Filmtabletten wurden bekannt gegeben.
 mehr...
mehr...

30. Januar 2026
Erstes Medikament gegen Non-CF-Bronchiektasen
Die EU-Zulassung von Brinsupri® markiert einen Meilenstein in der Therapie von Non-CF-Bronchiektasen.
 mehr...
mehr...

28. Januar 2026
Rote-Hand-Brief: Digitoxin
Geringfügige Überschreitung der Spezifikationsgrenze bei der Summe der Abbauprodukte am Haltbarkeitsende bei Digimerck minor.
 mehr...
mehr...

28. Januar 2026
Informationsbrief: Odronextamab
Rückruf von Ordspono® (Odronextamab) 80 mg IFK (Charge 8528300001): mangelhafte Verschlussintegrität der Durchstechflasche.
 mehr...
mehr...

21. Januar 2026
Rote-Hand-Brief: Infliximab
Neue i.v.-Formulierung Remsima® 100 mg & 350 mg enthält Sorbitol und ist bei hereditärer Fruktoseintoleranz kontraindiziert.
 mehr...
mehr...

15. Januar 2026
Neuer PD-1-Inhibitor Toripalimab verfügbar
Loqtorzi® steht als neue Therapieoption bei Nasopharynxkarzinom und Plattenepithelkarzinom des Ösophagus zur Verfügung.
 mehr...
mehr...

5. Januar 2026
Rote-Hand-Brief: Carbamazepin
Tegretal Suspension (Carbamazepin): Einschränkung der Anwendung bei Neugeborenen aufgrund Propylenglykol-Konzentration.
 mehr...
mehr...

16. Dezember 2025
Rote-Hand-Brief: Melphalanhydrochlorid
Melphalan AqVida 90 mg/ml IFK: potenzielles Risiko einer Überdosierung aufgrund einer höheren Konzentration.
 mehr...
mehr...

11. Dezember 2025
Rote-Hand-Brief: Tranexamsäure (intravenös)
Intravenöse Tranexamsäure-Formulierungen: schwere, teils tödliche Nebenwirkungen aufgrund versehentlicher intrathekaler Gabe.
 mehr...
mehr...

1. Dezember 2025
Olezarsen: erste Therapie speziell bei FCS
Tryngolza® wurde als erstes Arzneimittel speziell für das genetisch bestätigte familiäre Chylomikronämie-Syndrom zugelassen.
 mehr...
mehr...

10. November 2025
Informationsbrief: Cemiplimab
Chargennummer / Verfallsdatum können nach Desinfektion und Abwischen des LIBTAYO®-Etiketts unleserlich werden.
 mehr...
mehr...

7. November 2025
Rote-Hand-Brief: Phenytoin-Natrium
Bei der Charge 021950 des Produktes Phenhydan® Injektionslösung besteht das Risiko von Partikeln in den Ampullen.
 mehr...
mehr...

31. Oktober 2025
Romvimza®: Neu bei symptomatischem TGCT
Erstes zugelassenes Arzneimittel für die Behandlung des symptomatischen tenosynovialen Riesenzelltumors in der EU verfügbar.
 mehr...
mehr...

15. Oktober 2025
Ogsiveo®: Neu zur Therapie von Desmoidtumoren
Mit Ogsiveo® steht das erste zugelassene Arzneimittel für die Behandlung von Desmoidtumoren zur Verfügung.
 mehr...
mehr...

9. Oktober 2025
Rote-Hand-Brief: Burosumab
Information über das Risiko einer schweren Hyperkalzämie bei Patienten, die mit Crysvita® behandelt werden.
 mehr...
mehr...

9. Oktober 2025
Rote-Hand-Brief: Caspofungin
Die Verwendung von Polyacrylnitril-Membranen bei der kontinuierlichen Nierenersatztherapie sollte vermieden werden.
 mehr...
mehr...

26. September 2025
Rote-Hand-Brief: Lecanemab
Aktualisierung der Magnetresonanztomographie (MRT)-Zeitpunkte zur Ergänzung einer MRT vor der dritten Infusion von Leqembi®.
 mehr...
mehr...

18. September 2025
Rote-Hand-Brief: Chikungunya-Impfstoff
Aufhebung der vorübergehenden altersbezogenen Kontraindikation für IXCHIQ® und Information zu schwerwiegenden Nebenwirkungen.
 mehr...
mehr...

15. September 2025
Rote-Hand-Brief: Finasterid, Dutasterid
Neue Maßnahmen zur Minimierung des Risikos für Suizidgedanken bei Anwendung von Finasterid und Dutasterid.
 mehr...
mehr...

15. September 2025
Resmetirom: Erste zugelassene Therapie bei MASH
Mit Rezdiffra® steht erstmals ein Arzneimittel bei metabolisch Dysfunktions-assoziierter Steatohepatitis zur Verfügung.
 mehr...
mehr...

11. September 2025
Rote-Hand-Brief: Isoniazid Infusionslösung
ISOZID® 0,5 N: Risiko durch sichtbare Partikel und Verwendung eines Infusionsgeräts mit integriertem Partikelfilter.
 mehr...
mehr...

8. September 2025
Rote-Hand-Brief: Clozapin
Überarbeitete Empfehlungen zur routinemäßigen Blutbildkontrolle im Hinblick auf das Risiko einer Agranulozytose.
 mehr...
mehr...

1. September 2025
Weiteres Fumarat zur MS-Therapie verfügbar: RIULVY®
Tegomilfumarat ist zugelassen zur Behandlung von Patienten ab 13 Jahren mit schubförmig remittierender Multipler Sklerose (RRMS).
 mehr...
mehr...

29. August 2025
Rote-Hand-Brief: Fettemulsion
Lipidem® Emulsion zur Infusion: Hinweise zu subvisuellen Agglomeraten; Verwendung eines Infusionsfilters für Fettemulsionen.
 mehr...
mehr...

25. August 2025
Informationsbrief: Betain
Amversio® 1 g Pulver zum Einnehmen: Drei Chargen wurden mit veralteter PZN-Nummer in der NTIN-DE und im 2D-Barcode verpackt.
 mehr...
mehr...

21. August 2025
Rote-Hand-Brief: Evrysdi® 0,75 mg/ml Pulver zur Herstellung einer Lösung zum Einnehmen (Risdiplam)
Evrysdi® 0,75 mg/ml PLE: Fehlende Pflichtangabe auf Etikett, Faltschachtel, Rekonstitutionsanleitung und Fachinformation.
 mehr...
mehr...

1. August 2025
Neue Dreierkombination bei Mukoviszidose
Alyftrek® ermöglicht Patienten mit Mukoviszidose eine neue CFTR-Modulator-Kombination zur einmal täglichen Einnahme.
 mehr...
mehr...

11. Juli 2025
Neue Therapieoption bei Phenylketonurie
Mit Sephience® steht für Patienten mit Phenylketonurie eine weitere medikamentöse Behandlungsoption zur Verfügung.
 mehr...
mehr...

13. Juni 2025
Siiltibcy®: Neuer Tuberkulose-Hauttest
Ein neuartiges Diagnostikum zum intradermalen Nachweis von Mycobacterium tuberculosis-Infektionen kommt auf den Markt.
 mehr...
mehr...

23. Mai 2025
Arzneimitteltherapiesicherheit: Hätten Sie es gewusst?
Frau Schulz (71 Jahre) ist langjährige Patientin und erhält eine gut verträgliche Dauermedikation, darunter Tiotropiumbromid 10 µg (1-0-0) und Tramadol 100 mg retard (1-0-1). Die Patientin kommt in die Praxis und berichtet über neu aufgetretenen Schwindel sowie ein unangenehmes, trockenes Gefühl im Mund. Auf Nachfrage teilt Frau Schulz mit, dass sie seit über einem Monat täglich Cetirizin 10 mg, ein Arzneimittel gegen Heuschnupfen, aus der Apotheke einnimmt; ansonsten habe sich an ihrer Medikation nichts verändert.
 mehr...
mehr...

22. Mai 2025
Rote-Hand-Brief: Chikungunya-Impfstoff (lebend)
Für Ixchiq® gilt, während eine EU-weite Überprüfung läuft, eine neue Kontraindikation für Patienten ab 65 Jahren.
 mehr...
mehr...

20. Mai 2025
Informationsbrief: Obidoximchlorid
Toxogonin® (Obidoximchlorid) 250 mg/ml Injektionslösung: Informationsschreiben bezüglich Änderung der Lagerungsbedingungen.
 mehr...
mehr...

14. Mai 2025
Epinephrin als Notfall-Nasenspray
ALK-Abelló bringt mit EURneffy® das erste nadelfreie Notfallmedikament zur Anaphylaxie-Behandlung auf den EU-Markt.
 mehr...
mehr...

1. Mai 2025
Bevacizumab: Zulassung bei feuchter AMD
Mit Lytenava® ist das erste zugelassene Bevacizumab-Produkt für die ophthalmische Anwendung auf dem EU-Markt erhältlich.
 mehr...
mehr...

25. April 2025
Rote Hand Brief: Ruxolitinibphosphat
Wichtige Informationen zu möglichen enthaltenen Partikeln in Opzelura® 15 mg/g Creme (Ruxolitinibphosphat).
 mehr...
mehr...

23. April 2025
Rote-Hand-Brief: Distickstoffmonoxid/Sauerstoff
Risiko von Gasleck oder Versorgungsunterbrechung durch Ventilvereisung bei kontinuierlichem Fluss >8 l/min am Schlauchnippel.
 mehr...
mehr...

14. April 2025
Belzutifan: Erster oraler HIF-2a Inhibitor
Neue Therapieoption bei vorbehandeltem fortgeschrittenem Nierenzellkarzinom sowie Tumoren bei von-Hippel-Lindau-Erkrankung.
 mehr...
mehr...

31. März 2025
Beyonttra®: Neues Herzmedikament auf dem Markt
Neue Therapieoption der Wildtyp- oder hereditären Transthyretin-Amyloidose mit Kardiomyopathie bei Erwachsenen verfügbar.
 mehr...
mehr...

13. März 2025
Nemluvio®: Neu auf dem europäischen Markt
Eine neue Therapieoption für Patienten mit atopischer Dermatitis und Prurigo nodularis ist ab sofort verfügbar.
 mehr...
mehr...

28. Februar 2025
Rote Hand Brief: Aztreonam/Avibactam
Emblaveo® Pulver zur Herstellung einer Infusionslösung: Risiko von rissigen oder zerbrochenen Durchstechflaschen.
 mehr...
mehr...

28. Februar 2025
Neuer CGRP-Rezeptorantagonist zur Migräneprophylaxe
Mit Aquipta® kommt der erste einmal täglich einzunehmende CGRP-Rezeptorantagonist zur Migräneprophylaxe auf den Markt.
 mehr...
mehr...

17. Februar 2025
Informationsbrief: Ribociclib
Änderung der Lagerungsbedingungen und Haltbarkeit beim Präparat Kisqali® 200 mg Filmtabletten (Ribociclib).
 mehr...
mehr...

11. Februar 2025
Neues Target in der Hämophilie-Behandlung
Mit Hympavzi® bringt Pfizer einen neuen Wirkmechanismus für die Behandlung von Patienten mit Hämophilie A und B ins Spiel.
 mehr...
mehr...

15. Januar 2025
Neueinführung Casgevy®
Die neue Zelltherapie Exagamglogen autotemcel verspricht Hoffnung bei Beta-Thalassämie und Sichelzellkrankheit.
 mehr...
mehr...

13. Januar 2025
Rote-Hand-Brief: Fezolinetant
Risiko für arzneimittelbedingten Leberschaden und neue Empfehlungen zur Überprüfung der Leberfunktion.
 mehr...
mehr...

20. Dezember 2024
Neuzulassung Elahere®
Neue Therapieoption, speziell für Patientinnen mit Folatrezeptor-alpha(FRa)-positivem, platinresistentem Eierstockkrebs.
 mehr...
mehr...

20. Dezember 2024
Rote-Hand-Brief: Darvadstrocel
Alofisel® (Darvadstrocel): Rücknahme vom EU-Markt, da der klinische Nutzen nicht mehr nachgewiesen ist.
 mehr...
mehr...

9. Dezember 2024
Rote-Hand-Brief: Hydroxycobalamin
Qualitätsmangel bei Cyanokit wegen möglicher mikrobieller Kontamination und des potenziellen Infektionsrisikos.
 mehr...
mehr...

9. Dezember 2024
Rote-Hand-Brief: Metamizol
Metamizolhaltige Arzneimittel: Wichtige Maßnahmen zur Minimierung der schwerwiegenden Folgen des Risikos für Agranulozytose.
 mehr...
mehr...

2. Dezember 2024
Einführung eines neuen mRNA-Impfstoffs gegen RSV
Mit mRESVIA steht älteren Patienten ein dritter Impfstoff zur Verfügung, um schwere Krankheitsverläufe zu vermeiden.
 mehr...
mehr...

25. November 2024
Arznei aktuell: Neues Release ist da!
Mit der neuen Version von Arznei aktuell legen wir besonderen Wert auf Sicherheit. Entdecken Sie neue Funktionen wie eine praktische Abmeldefunktion, ein automatisches Löschkonzept für inaktive Konten und erhöhte Passwortanforderungen. Erfahren Sie, wie diese Verbesserungen Ihre Nutzung der Anwendung noch sicherer machen!
 mehr...
mehr...

11. November 2024
Vyloy: Neue Option bei Magenkarzinomen
Neueinführung von Zolbetuximab zur Behandlung von Adenokarzinomen des Magens und des gastroösophagealen Übergangs.
 mehr...
mehr...

31. Oktober 2024
Europaweite Markteinführung von Artesunat
Amivas bringt die einzige zugelassene parenterale Therapie gegen schwere Malaria auf den deutschen Markt.
 mehr...
mehr...

24. Oktober 2024
Rote Hand Brief: 5-Fluorouracil (i.v.)
Messung des Uracilspiegels mit Vorsicht interpretieren bei Patienten mit mittelschwerer oder schwerer Nierenfunktionsstörung.
 mehr...
mehr...

23. Oktober 2024
Informationsschreiben: Insulinangebot
Wichtige Informationen für Ärzt:innen zu einer Anpassung des Insulinangebotes von Novo Nordisk in Deutschland.
 mehr...
mehr...

14. Oktober 2024
Neue Therapie für die primäre biliäre Cholangitis
Iqirvo® (Elafibranor) wurde als Zweitlinientherapie für die Behandlung der primär biliären Cholangitis (PBC) zugelassen.
 mehr...
mehr...

9. Oktober 2024
Rote Hand Brief: Medroxyprogesteronacetat
Meningeomrisiko bei Einnahme von hochdosiertem Medroxyprogesteronacetat und Maßnahmen zur Minimierung dieses Risikos.
 mehr...
mehr...

7. Oktober 2024
Rote-Hand-Brief: Voxelotor
Ruhen der Genehmigung für das Inverkehrbringen von Oxbryta® in der Europäischen Union als Vorsichtsmaßnahme.
 mehr...
mehr...


Arzneimittel-Therapie-Sicherheit
Rote-Hand-Brief Azacitidin
Erweiterung des Produktportfolios birgt das Risiko für Medikationsfehler.
 mehr...
mehr...
11. Juni 2017, Med-News - @rzneimittelnews.de
Große Datenbank-Analyse: NSAID erhöhen Herzinfarktrisiko schon in der ersten Woche
Eine große Metaanalyse hat es jetzt erneut bestätigt: Die Einnahmen von nicht steroidalen Antiphlogistika (NSAID) ist dosisabhängig mit einem signifikant erhöhten Herzinfarktrisiko verbunden – und das bereits in der ersten Therapiewoche.
Für die Metaanalyse wählten kanadische Wissenschaftler die allgemeine digitale Versicherungsdatenbank in Quebec, eine populationsbasierte Fall-Kontroll-Studie aus Finnland sowie zwei "Nested Case Control Studies" aus Großbritannien und Kanada. Die gepoolten Daten umfassten 61.460 Fälle von Herzinfarkten und 385.303 Kontrollen bei insgesamt 446.763 Individuen. Bei den analysierten NSAID handelte es sich um Celecoxib, die 3 wichtigsten klassischen NSAID Diclofenac, Ibuprofen und Naproxen.
Insgesamt lag bei aktuellem NSAID-Gebrauch die Zunahme des Infarktrisikos gegenüber keinem Gebrauch bei 20 bis 50%. Diese signifikante Erhöhung des Infarktrisikos zeigte sich bei den klassischen NSAID Ibuprofen (OR 1,50) Diclofenac (OR 1,48) und auch Naproxen (OR 1,53), das als eines der sichersten Vertreter der Klasse gilt. Das Risiko für Celecoxib (OR 1,24) war nicht größer als das der klassischen NSAID. Die Risikoerhöhung zeigte sich bereits in der ersten Therapiewoche, was die Autoren eher nicht erwartet hatten.
Höhere Dosen waren auch mit einem erhöhten Infarktrisiko assoziiert. Die Einnahme einer hohen Dosis über 8 bis 30 Tage war besonders nachteilig für Ibuprofen (> 1.200 mg/d), Naproxen (> 750 mg/d). Eine darüber hinausgehende Behandlungsdauer schien mit keiner weiteren Zunahme des Risikos in Zusammenhang zu stehen – das Risiko nahm aber auch nicht ab.
Für die meisten Patienten sei das Risiko jedoch sehr gering. Mittelt man Personen mit verschiedenen kardialen Risiken, liegt das spezifische Risiko durch eine NSAID-Einnahme bei lediglich 1% pro Jahr. Auf 100 Personen, die kontinuierlich über ein Jahr behandelt werden, kommt somit ein zusätzlicher Herzanfall.
Trotzdem sollten Ärzte nicht nur die kleinstmögliche NSAID-Dosierungen für den kürzest möglichen Zeitraum verordnen, sondern ihre Patienten auch über ihre kardialen Risiken aufklären, empfehlen die Autoren.


Rote-Hand-Brief zu Adempas® (Riociguat):
Neue Kontraindikation für Patienten mit pulmonaler Hypertonie in Verbindung mit idiopathischen interstitiellen Pneumonien (PH-IIP)
Die Firmen Bayer AG und MSD Sharp & Dohme GmbH informieren in einem Rote-Hand-Brief zu Adempas® über Zwischenergebnisse der Studie RISE-IIP in der Patienten ...
 mehr...
mehr...
Herausgeber
Ärztenetzwerk coliquio - Die medizinische Online-Community
Internet www.coliquio.de


Welcome to CredibleMeds®
CredibleMeds® drugs lists are free to registered users.
Registration is required so we can notify users when the lists are revised. Use of out-of-date lists can be dangerous.
Internet crediblemeds.org
1. März 2018
New drugs and New Features to QTdrugs
We are writing to inform you that we have added the following three drugs to the QTdrugs lists.
Tramadol, a medicine for pain, has been added to the Possible Risk of Torsades de Pointes (TdP) category due to evidence that it is associated with QT prolongation when taken at clinically recommended doses.
Propafenone, a medicine used to treat heart rhythm disturbances, and Metolazone, a diuretic, have been added to the Conditional Risk list because they have been associated with TdP under certain conditions.
Also, we are reminding you of Two New Features for QTdrugs Search and Display.
1. Search Drugs by Market Status
Visitors to the CredibleMeds.org website can now tailor their drug searches and downloads to include only those drugs that are on the market worldwide, those removed from the market or those marketed only in the US. Simply set filters for the drugs to be displayed by clicking one of the radio buttons now found below the list of TdP Risk Categories (See choices underlined in red in screenshot below).
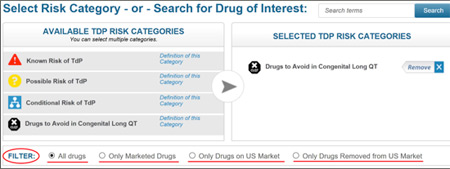
2. New Drug Label Information for Healthcare Providers
CredibleMeds can now inform users when the FDA label for drugs marketed in the US includes a recommendation for prescreening ECGs, monitoring ECG during therapy or if the recommendation is specific for certain conditions, e.g. overdose. While displaying a QTdrugs list, click on a drug and a pop-up shows you this and other essential information about the drug. See screenshot below. Note that this information regarding recommendations for ECG monitoring is only available for drugs that are marketed in the US.
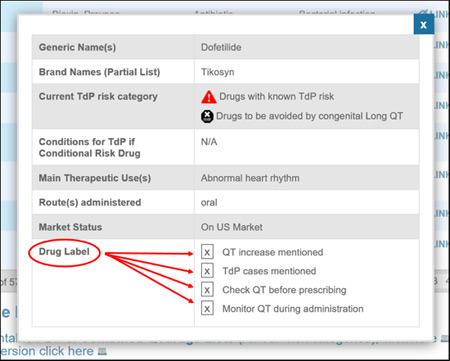
These additions to the website are the direct result of feedback we have received from users. Please continue to send your suggestions for how the CredibleMeds website and its QTdrugs lists can better serve your needs.
Thank you for your interest in CredibleMeds.org.
Sincerely,
Raymond L. Woosley, MD, PhD
Klaus Romero, MS, MD
Will Heise, MD


Herausgeber
Springer Medizin - Das Fachportal für Ärzte
Internet www.springermedizin.de
Artikel vom 23. Juli 2014
Prof. Dr. med. Bernd Pötzsch:
"Damit das Blut nicht in den Adern stockt ... - Neue orale Antikoagulanzien oder doch Marcumar?"
Im ambulanten Bereich hat die Zahl der verordnungsfähigen Antikoagulanzien zugenommen und wird weiter wachsen. Für den Hausarzt stellt sich dadurch die Frage, welche Kriterien und präparatespezifischen Eigenschaften die Antikoagulanzienauswahl bestimmen können.
Quelle:
MMW - Fortschritte der Medizin
Quellendetails:
Zeitschrift: MMW - Fortschritte der Medizin 2014/9: 48-56
Autor: Prof. Dr. med. Bernd Pötzsch (Universitätsklinikum Bonn)
DOI: 10.1007/s15006-014-2868-2
Artikel:
 www.springermedizin.de
www.springermedizin.de